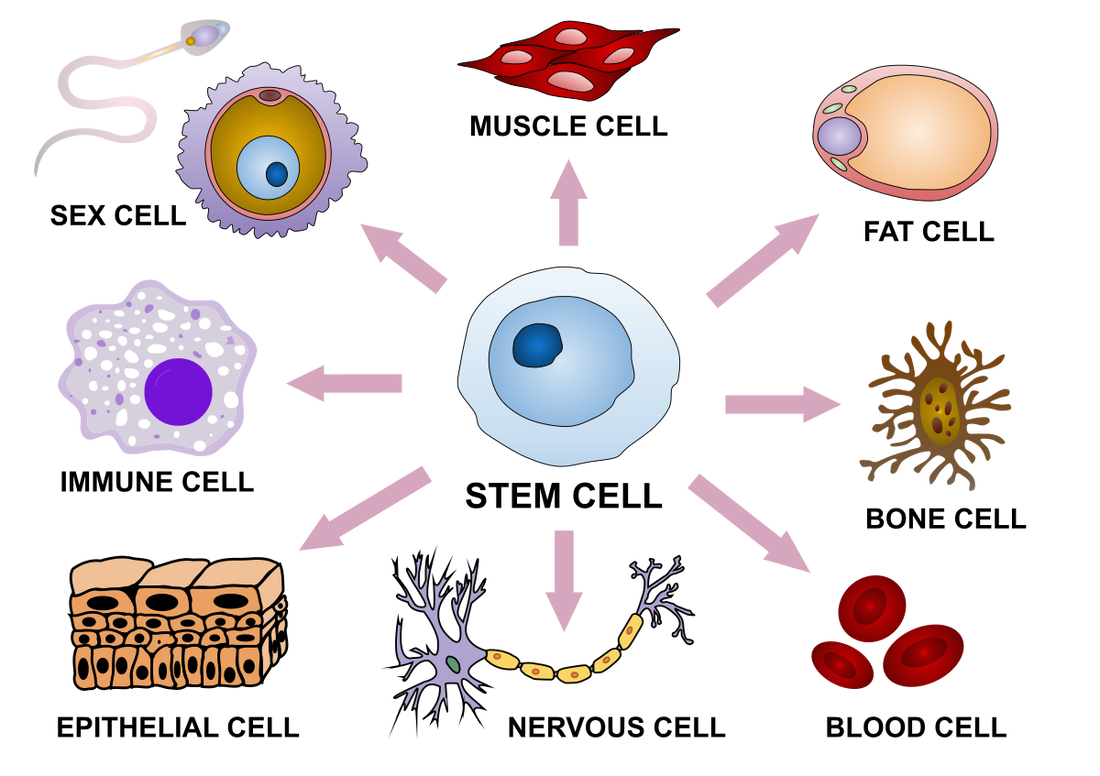
Sigurno ti je poznato da sve ćelije jednog organizma imaju isti genetički materijal odnosno istu dnk. Međutim nemaju sve ćelije istu funkciju. Ipak neke procese obavljaju sve ćelije, a neke samo pojedine.
Ćelije se međusobno razlikuju po poreklu,veličini, obliku i funkciji. U jednom organizmu možemo razlikovati više od stotinu vrsti ćelija. Aktivnosti koje su zajedničke za sve vrste ćelija nazivamo osnovnim ćelijskim procesima ili funkcijama. Ćelijske funkcije nastaju iz specifičnog ćelijskog poretka tokom kojih se u organelama odvijaju pojedinačni ćelijski procesi, koji su međusobno povezani na način da se održi stalnost unutrašnje sredine i celovitost ćelije. Osnovni ćelijski procesi obezbeđuju održavanje celovitosti ćelije i njenog života. Na primer nervna ćelija i ćelija jetre imaju sličan način razmenjivanja hranljivih materija sa neposrednom vanćelijskom okolinom, takođe sve vrste ćelija vrše proces ćelijskog disanja, sinteze proteina itd.
Pored osnovnih životnih procesa, ćelije mogu da obavljaju više specijalizovanih ćelijskih procesa.. Specijalizovani ćelijski procesi nastaju procesom specijalizacije , oni zajedno sa aktivnostima drugih ćelija datog tkiva i organa održavaju organizam kao celina. Na primer uloga eritrocita je u prenošenju kiseonika i drugih hranljivih materija, dok je uloga leukocita odbranbenog karaktera.
Sve ćelije (prokariotske i eukariotske) su odvojene od spoljašnje sredine ćelijskom membranom. Unutrašnjost ćelija je ispunjena citosolom- vodenim rastvorom koji je obogaćen kalijumom. U eukariotskim ćelijama prisutne su funkcionalne jedinice koje su posebno odvojene svojom membranom od ostatka ćelije, koje nazivamo ćelijskim organelama. U ćelijske organele ubrajamo mitohondrije,lizozome,jedro itd. Citoplazma predstavlja unutrašnji sadržaj ćelije, odvojen od jedra, u kome se nalaze ćelijske organele. Citoplazmu, dakle, čine citosol i ćelijske organele. Citosol je deo citoplazme van ćelijskih organela koji zauzima oko 55% ukupne ćelijske zapremine.
Ćelijske organele od ostatka citoplazme mogu biti odvojene jednom membranom (jednomembranske) ili dvema membranama (dvomembranske).Membrane kojima su organele odvojene obezbeđuju izdvojenu lokalnu sredinu koja olakšava odigravanje specifičnih procesa, koji se ne mogu odigravati u citoplazmi uporedno sa drugim procesima.
Enzimi u lizozomima optimalno funkcionišu u kiselon sredini (ph<7), koja se uspostavlja neprestanim unošenjem H+ jona iz citosola u lizozom. Ukoliko bi sadržaj lizozoma iscurio iz lizozoma, on bi uništio unutraćelijske strukture i doveo do ćelijske smrti. Zbog toga je važno da se obezbedi optimalna sredina za odvijanje svih ćelijskih procesa.
Iako su organele odvojene od citosola svopstvenom membranom, procesi koji se odvijaju u njima ne funkcionišu izolovano,već kordinisano kao jedna celina.
Međusobnu kordinaciju procesa u ćeliji objasnićemo na primeru neurona i prenošenja inpulsa. Ukoliko želiš da saznaš više o ovj temi istraži na internetu o protoku genetičke informacije kroz ćeliju.
Uloga nervne ćelije je prenos signala -nervnih inpulsa do drugih ćelija u organizmu. Taj cilj postižu sintezom i transportom (otpuštanjem) posebnih hemijskih glasnika odnosno neurotransmitera. U ovom procesu učestvuju gotovo svi delovi ćelije.
- Kako su neurotransmiteri proteinske prirode, informacije za sintezu proteina smeštene su u DNK koji se nalazi u hromozomima jedra.
- U ribozomima koji se nalaze u endoplazmatičnom retikulumu se vrši sinteza proteina.
- Dobijeni proteini (neurotransmitori) se modifikuju i pakuju u sinaptičke vezikule pod kontrolom Goldžijevog aparata.
- Elementi citoskeleta transportuju vezikule do mesta sa kojeg će se osloboditi.
- Neurotransmitori se primaju pomoću posebnih receptora na ćelijskoj membrani koja stvara akcione potencijale i na taj način prenosi inpuls.
- Mitohondrije obezbeđuju neophodnu energiju za sve ove procese.
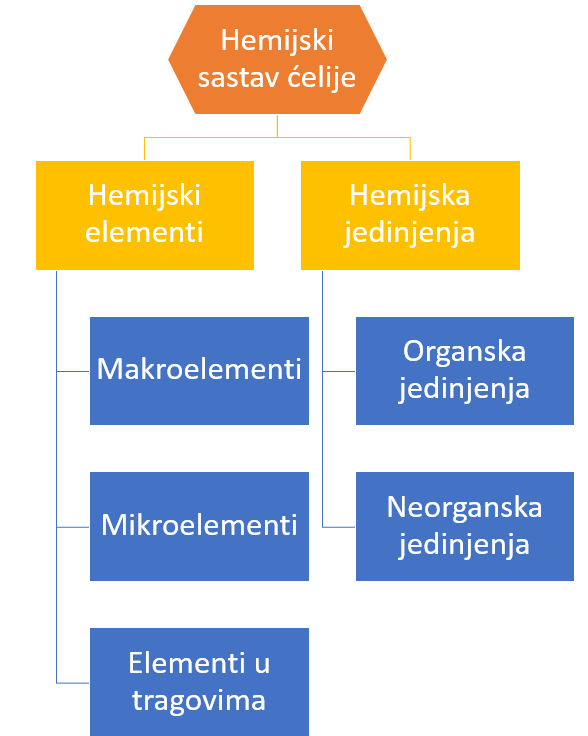
Kao i sve ostalo u prirodi i ćelija je izgrađena od materije. Materija od koje je izgrađena ćelija deli se na hemijske elemente i hemijska jedinjenja.
Procentualna zastupljenost elemenata u živoj i neživoj prirodi je veoma različita. Od 92 hemijskih elemenata koji su prisutni u prirodi samo 25 je potrebno za organizaciju života. Zbog obaveznog prisustva ovih elemenata u živoj materiji nazivamo ih biogenim elementima (bios-život, genesis-postanak).
Biogene elemente na osnovu procentualne zastupljenosti u ćeliji delimo na:
- Makroelemente
- Mikroelemnte
- Elemente u tragovima
Podseti se lekcije o primanju mineralnih elemenata kod biljaka i njihovoj funkciji:https://biologija-gimnazija.weebly.com/primanje-mineralnih-elemenata-i-njihove-funkcije.html
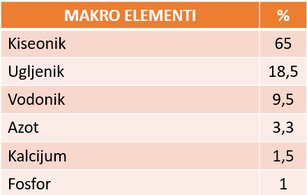
Od svih biogenih elemenata samo ugljenik (C), kiseonik (O), vodonik (H) i azot (N) čine 96% žive materije. Ova četiri elemenata zajedno sa kalcijumom (Ca) i fosforom (P) koji ulaze u sastav egzoskeleta i endoskeleta spadaju u makroelemente.
Makroelementi učestvuju u izgradnji 98% žive materije.
Makroelementi učestvuju u izgradnji 98% žive materije.
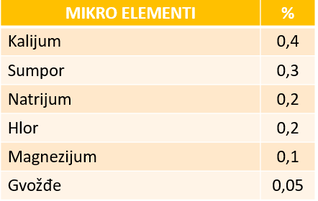
Mikroelementi se nalaze u znatno manjim količinama od makroelemenata, ali je njihovo prisustvo u živim bićima neophodno za normalno odvijanje životnih procesa. U mikroelemente spadaj: sumpor (ulazi u sastav amino-kiselina i proteina), kalijum, natrijum i hlor (imaju ulogu u održavanju membranskog potencijala i prenošenja akcionog potencijala), magnezijuma (sastavni deo enzima kod životinja, a kod biljaka deo hlorofila) kao i gvožđe (gradivna komponenta hemoglobina).

Pored makroelemenata i mikroelemenata u ćelijama su prisutni elementi u tragovima, koji ukupno čine manje od 0,01% mase svih živih materija.Njihov se nedostatak u prehrani očituje celim nizom naizgled beznačajnih oštećenja, ali na kraju ipak ozbiljnih, pa čak i smrtonosnih. Neki naučnici smatraju da su minerali važniji od vitamina, jer se u živom organizmu gotovo nikako ne mogu stvoriti.
Cink, bakar i magnezijum važni su minerali koji nas štite od stresa (naročito magnezijum), održavaju našu kožu i kosu nežnom (naročito cink) i sprečavaju nastanak anemije (naročito bakar - pomaže gvožđu prilikom stvaranja crvenih krvnih zrnaca). Ova tri elementa nedostaju kod žena koje pate od tzv. predmenstrualnog sindroma, imaju krhku kosu, nokte i tanku kožu, a njihov se nedostatak uz gvožđe, može javiti i kod obilnih menstrualnih krvarenja.
Jod je važan jer omogućava nesmetan rad štitne žlezde. Nedostatak joda izaziva gušavost.
Cink, bakar i magnezijum važni su minerali koji nas štite od stresa (naročito magnezijum), održavaju našu kožu i kosu nežnom (naročito cink) i sprečavaju nastanak anemije (naročito bakar - pomaže gvožđu prilikom stvaranja crvenih krvnih zrnaca). Ova tri elementa nedostaju kod žena koje pate od tzv. predmenstrualnog sindroma, imaju krhku kosu, nokte i tanku kožu, a njihov se nedostatak uz gvožđe, može javiti i kod obilnih menstrualnih krvarenja.
Jod je važan jer omogućava nesmetan rad štitne žlezde. Nedostatak joda izaziva gušavost.
U narednim prezentacijama možeš se upoznati sa značajem svakog pojedinačnog elementa i njegovim dejstvom na živa bića.
|
| ||||||||||||
Život na zemlji je nastao u vodi i voda danas predstavlja prirodno stanište mnogim živim bićima. Veoma je slična zastupljenost vode u prirodi i u organizmima. Ona je pretežni sastojak citosola i vanćelijskih tečnosti.
Voda je najznačajnije neorgansko jedinjenje za funkcionisanje ćelije. Voda je toliko uobičajna i široko rasprostranjena u prirodi da često zaboravimo da je voda u velikoj meri izuzetna supstanca , od koje zavise svi oblici života na zemlji. Mnoge biološke funkcije vode proističu iz njene fizičke strukture i nekih fizičkih osobina svojstvenih samo za nju.
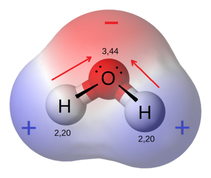
U molekulu vode, atomi vodonika i kiseonika dele elektrone formirajući kovalentne veze. Kiseonik je elektronegativniji od vodonika te se elektroni nalaze bliže molekulu kiseonika. Međutim, usled toga što neravnomerno dele elektrone iako je totalno naelektrisanje vode neutralno voda je polarni molekul. Polarna priroda vode omogućava joj da rastvara polarne supstance , kao što su šećeri ,soli i neke proteine.
Similia similibus solvuntur-Slično se u sličnom rastvara
Molekuli koji se rastvaraju u vodi nazivaju se hidrofilni (u prevodu: vole vodu). Kako je voda polarna a shodno principu u hemiji slično se u sličnom rastvara, voda ne rastvara nepolarna jedinjenja kao što su ulja i masti (lipidi) ili ih delimično rastvara. Takva jedinjenja nazivamo hidrofobnim (u prevodu: plaše se vode).
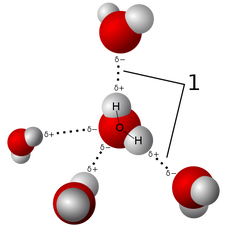
7Polarni molekuli se međusobno privlače. Tako elektropozitivniji vodoonični deo jednog molekula privlači elektronegativnije kiseonične delove drugih molekula.Ovakva vrsta privlačenja se naziva vodonična veza. Svaki molekul vode može vezati vodoničnim vezama do četiri susedna molekula vode. Vodonične veze u vodi ispoljavaju dovoljno jake privlačne sile tako da voda može " da se drži sama za sebe".
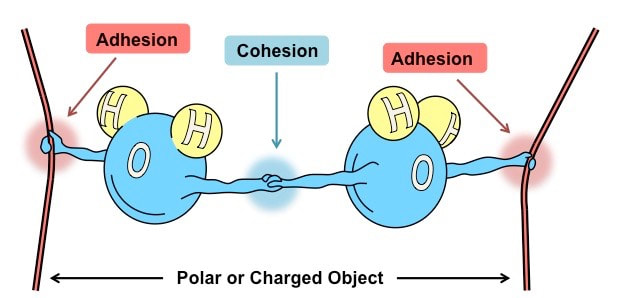
Privlačna sila koja drži molekule jedne supstance zajedno naziva se kohezija. Kohezija kod biljaka utiče na kretanje vode od korenovog sistema do listova. Kada voda ispari sa lista , čitav stub se pomera na gore kao odgovor na povlačenje molekula na vrhu. Kohezija uzrokuje pojavu površinskog napona. Površinski napon formira neku vrstu opne na površini vode. Jedna od posledica površinskog napona jeste da manji insekti i pauci mogu da se kreću po vodi.
Privlačna sila koja drži molekule jedne supstance zajedno naziva se kohezija. Kohezija kod biljaka utiče na kretanje vode od korenovog sistema do listova. Kada voda ispari sa lista , čitav stub se pomera na gore kao odgovor na povlačenje molekula na vrhu. Kohezija uzrokuje pojavu površinskog napona. Površinski napon formira neku vrstu opne na površini vode. Jedna od posledica površinskog napona jeste da manji insekti i pauci mogu da se kreću po vodi.
Adhezija je privlačna sila između molekula 2 različite supstance (npr. molekula vode i stakla). Jedna od pojava koja je posledica adhezije jeste kapilarnost. Kapilarnost je privlačnost molekula koja uzrokuje podizanje površine tečnosti kada je u kontaktu sa čvrstom supstancom.
Više o koheziji, adheziji i kapilarnim pojavama učićeš u okviru časova fizike i hemije. Savetujemo ti da na linku istražiš više o fenomenu poznatom kao anomalije vode. |
Uloga vode u organizmima je višestruka i nezamenljiva. Kao rastvarač polarnih jedinjenja učestvuje u njihovom transportu kroz membranu i obezbeđuje sredinu za odigravanje svih tipova hemijskih reakcija u ćeliji. U procesu ćelijskog disanja u kome se dobija velika količina hemijske energije oslobađa se velika količina toplote. Voda apsorbuje tu toplotu i na taj način reguliše temperaturu ćelije. Takođe toplokrvni organizmi se hlade odavanjem vode. U tkivima ljudskog organizma procenat vode se kreće od 20% u koštanom tkivu do 85% u ćelijama mozga.
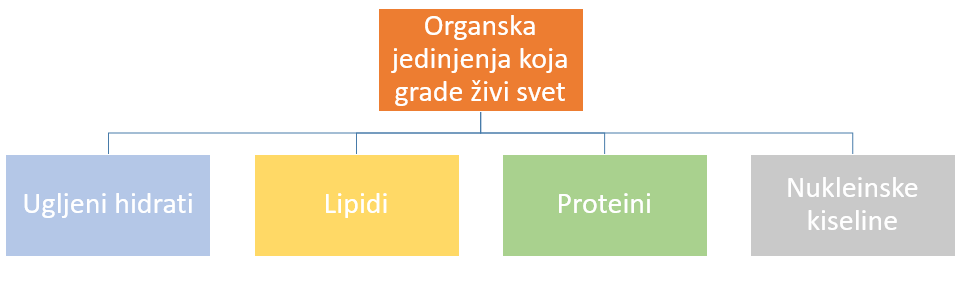
Sva živa materija u organizmima izgrađena je od samo četiri vrste organskih molekula. U organske molekule koji grade živi svet ubrajamo:ugljene hidrate,lipide, proteine i nukleinske kiseline.
Osim lipida sva ostala gradivna organska jedinjenja su polimeri, odnosno izgrađena su od više kovalentno povezanih manjih molekula odnosno monomera. Monomeri čija je molarna masa veća od 1 grama po molu nazivaju se makromolekulima.
Neosporno je da ugljene hidrate, proteine i nukleinske kiseline svrstavamo u makromolekule. Ali šta je sa lipidima?
Iako nisu polimeri, uobičajno je da se veliki lipidi tretiraju kao poseban tip makromolekula.
Za dalje razumevanje ove lekcije preporučujemo ti da se podsetiš uvodnih lekcija iz organske hemije. Podseti se šta je funkcionalna grupa i šta ona određuje. Takođe podseti se funkcionalnih grupa organskih jedinjenja koja su gradivni elementi zivih materija.
| Преглед функционалних група у органској хемији | |
| File Size: | 118 kb |
| File Type: | |
Ugljeni hidrati ili šećeri su najrasprostranjenija jedinjenja u živom svetu. Ugljeni hidrati su biološki molekuli koji se sastoje od atoma ugljenika (C), vodonika (H) i kiseonika (O), obično sa odnosom atoma ugljenika i kiseonika od 2:1 (kao u vodi); drugim rečima, sa empirijskom formulom Cm(H2O)n (gde se m može razlikovati od n). Postoje 3 kategorije biološki bitnih ugljenih hidrata a to su: monosaharidi, oligosaharidi i polisaharidi. Ugljeni hidrati su glavni izvor energije za sva živa bića. Osim toga oni imaju takođe strukturnu ulogu kao što je celuloza kod biljaka i hitin kod životinja.
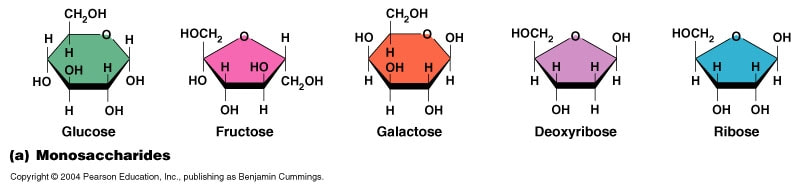
Prosti šećeri ili monosaharidi predstavljaju monomere od kojih se grade veći ugljeni hidrati. Biološki najznačajniji monosaharidi su pentoze i heksoze, ali to nisu jedine vrste monosaharida jer postoje i trioze, tetroze itd. Monosaharidi (prosti šećeri) se hidrolizom ne mogu razložiti na prostija jedinjenja.
Pentoze su monosaharidi sa pet ugljenikovih atoma.Pentozama pripadaju dva, biološki veoma značajna jedinjenja:
- riboza, ulazi u sastav RNK i
- dezoksiriboza koja gradi DNK.
Heksoze su monosaharidi sa šet ugljenikovih atoma. Najpoznatiji heksozni šećeri su glukoza, fruktoza i galaktoza. Glukozu ili grožđani šećer poseduju sva živa bića. Glukoza se koristi kao glavni izvor energije , jer se u toku ćelijskog disanja glukoza razlaže na vodu i ugljen dioksid uz oslobađanje energije. U slobodnoj formi nalazi se u voćnim sokovima i krvi. Fruktoza ili voćni šećer je najslađi šećer- monosaharid , a najmanje sladak monosaharid je galaktoza
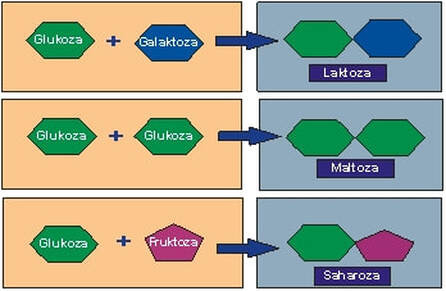
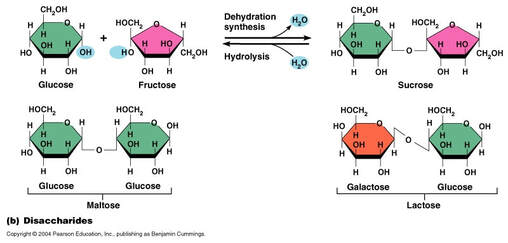
Oligosaharidi su građeni od 2 do 15 monosaharida povezanih glikozidnom vezom. Poseban slučaj oligosaharida su disaharidi koji su građeni od dva monosaharida. Biološki najznačajniji oligosaharidi su saharoza,laktoza i maltoza.
Maltoza ili sladni šećer građen je od dva molekula glukoze.
- Glukoza i fruktoza grade najpoznatiji šećer saharozu.
Maltoza ili sladni šećer građen je od dva molekula glukoze.
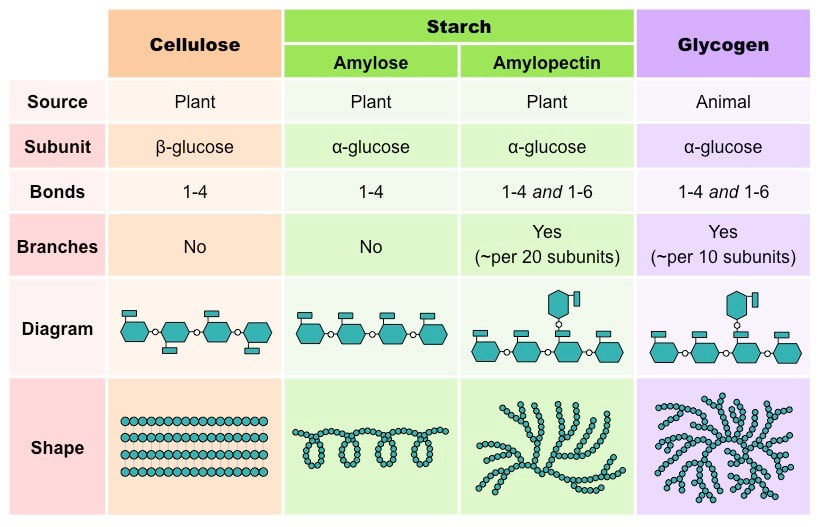
Polisaharidi su makromolekuli sastavljeni od velikog broja monosaharida povezanih glikozidnom vezom. Najpoznatiji polisaharidi su građeni isključivo od glukoze. Većinom nisu rastvorljivi u vodi i nemaju sladak ukus. Uloga polisaharida u organizmima može biti gradivna ili mogu služiti kao rezervna materija. Najznačajniji polisaharidi su : skrob, celuloza, glikogen i hitin.
Razlaganjem polisaharida- rezervnih materija nastaju molekuli glukoze. Kod životinja rezervna materija je glikogen, koji se kod čoveka i drugih kičmenjaka pretežno nalazi u ćelijama jetre i mišićnim ćelijama. Kod biljaka rezervna materija je skrob koji se u vidu granula nalazi u plastidima.
Polisaharidi koji imaju gradivne uloge služe kao gradivni materijali za strukture koje štite ćelije, ali i ceo organizam.
Biljke proizvode polisaharid celulozu koja izgrađuje čvrst ćelijski zid biljnih ćelija. Kao i skrob i celuloza je polimer glukoze, ali veze kojima su monomeri u molekulu glukoze povezani drugačije su u odnosu na skrob.Posledica toga je da enzimi za razgradnju skroba ne mogu da razgrade celulozu, te zbog toga celuloza prolazi nesvarena kroz crevni trakt čoveka i izbacuje se fecesom. Iako nema hranljivu vrednost za čoveka, celuloza ima značajnu ulogu u varenju. Naime celulozna vlakna stimulišu rad creva i olakšavaju prolazak hrane kroz crevni trakt.
Biljke proizvode polisaharid celulozu koja izgrađuje čvrst ćelijski zid biljnih ćelija. Kao i skrob i celuloza je polimer glukoze, ali veze kojima su monomeri u molekulu glukoze povezani drugačije su u odnosu na skrob.Posledica toga je da enzimi za razgradnju skroba ne mogu da razgrade celulozu, te zbog toga celuloza prolazi nesvarena kroz crevni trakt čoveka i izbacuje se fecesom. Iako nema hranljivu vrednost za čoveka, celuloza ima značajnu ulogu u varenju. Naime celulozna vlakna stimulišu rad creva i olakšavaju prolazak hrane kroz crevni trakt.
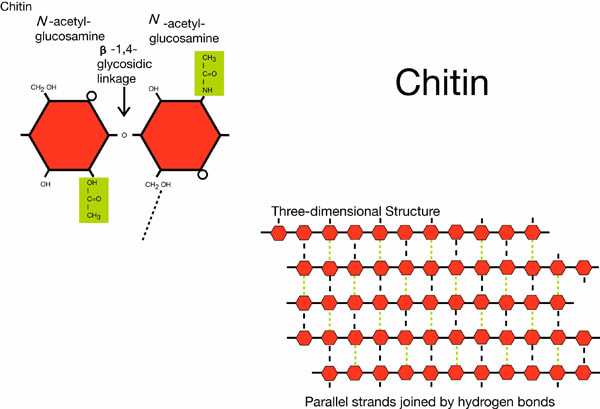
Strukturni polisaharid kod zglavkara je hitin. Čine ga lanci nastali povezivanjem modifikovanih molekula glukoze. Hitin gradi spoljašnji odnosno egzoskelet zglavkara. Egzoskelet je tvrd spoljašnji omotač, očvrsnut kristalima kalcijum karbonata, koji štiti meka tekiva životinje. Osim toga hitin se nalazi i u hifama nekih gljiva.
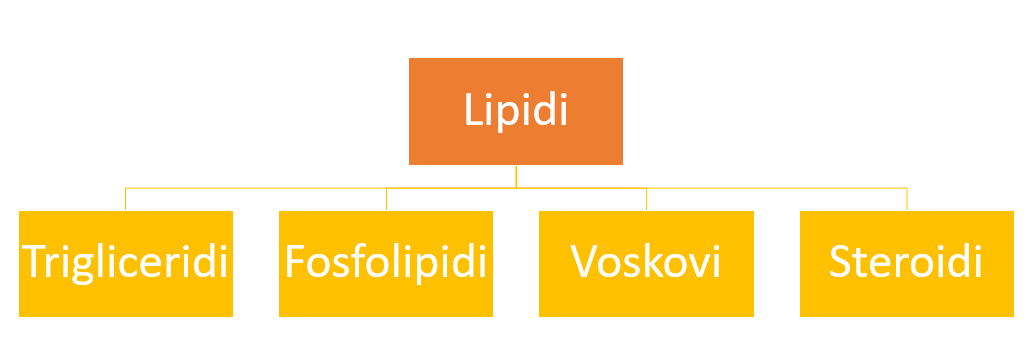
Lipidi su veliki, nepolarni, hidrofobni molekuli. Grupa lipida obuhvata: trigliceride, fosfolipide,steroide, voskove i određene pigmente. Za razliku od molekula ugljenih hidrata lipidi imaju više atoma ugljenika i vodonika.
| 22.-hemija-lipidi.pdf | |
| File Size: | 1504 kb |
| File Type: | |
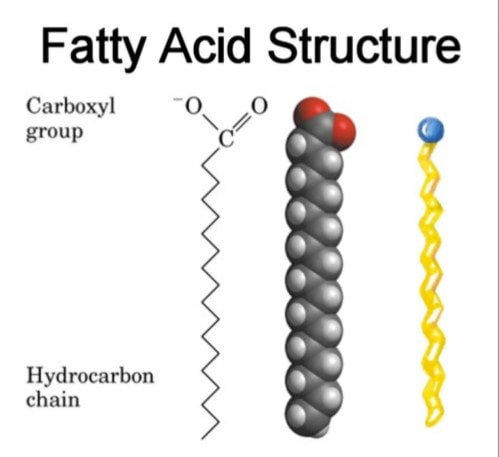
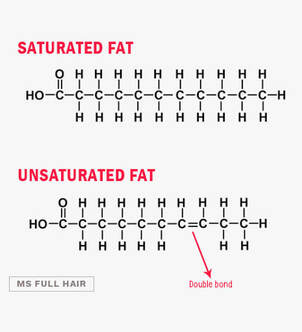
Masne kiseline su karboksilne kiseline sa dugim nerazgranatim ugljovodoničnim lancem. Masne kiseline su sastavni deo većine lipida. Masne kiseline se sastoje od karboksilnog dela koji je hidrofilan i ugljovodoničnog lanca koji je hidrofoban. Masne kiseline koje ulaze u sastav masti mogu imati različit broj atoma ugljenika. Masne kiseline mogu biti zasićene i nezasićene. Shodno tome one mogu imati različit broj dvostrukih veza. Zasićene masne kiseline nemaju dvostruke veze. Kod zasićenih masnih kiselina svaki (primer stearinska) ugljenikov atom je povezan sa još četiri druga atoma, te se zbog toga nazivaju zasićenim ili saturisanim. Nezasićene masne kiseline imaju bar 1 dvostruku vezu, a kiseline koje sadrže više dvostukih veza nazivamo polinezasićene masne kiseline. Nezasićene masne kiseline drugačijim nazivom se nazivaju i nesaturisane.
Trigliceridi ili masnoće su lipidi koji su građeni od tri molekula masnih kiselina i jednog molekula alkohola glicerola. Molekuli masnih kiselina su povezani estarskom vezom za molekul glicerola.
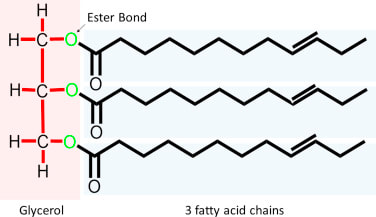
Na osnovu masnih kiselina koje ulaze u sastav triglicerida, trigliceridi se dele na zasićene i nezasićene.
Zasićeni trigliceridi imaju višu tačku topljenja i u čvrstom su agregatnom stanju. na sobnoj temperaturi. Nezasićeni trigliceridi imaju nižu tačku ključanja i na sobnoj temperaturi su uglavnom u tečnom stanju. Nezasićeni trigliceridi se uglavnom mogu naći u semenima biljaka gde služe kao izvor ugljenika i energije za biljke u razvoju. Preradom ili hladnim ceđenjem ovakvih semena dobijaju se biljna ulja.
Zasićeni trigliceridi imaju višu tačku topljenja i u čvrstom su agregatnom stanju. na sobnoj temperaturi. Nezasićeni trigliceridi imaju nižu tačku ključanja i na sobnoj temperaturi su uglavnom u tečnom stanju. Nezasićeni trigliceridi se uglavnom mogu naći u semenima biljaka gde služe kao izvor ugljenika i energije za biljke u razvoju. Preradom ili hladnim ceđenjem ovakvih semena dobijaju se biljna ulja.
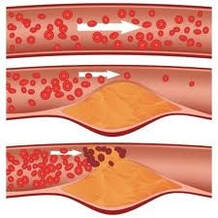
Zanimljivost: Svinjska mast i maslac su zasićene masti (trigliceridi) i zbog toga su čvrsti na sobnoj temperaturi. Masti riba i biljaka su uglavnom nezasićene i zbog toga su u tečnom stanju. Do sada ste se sigurno susreli sa pojom hidrogenizovana biljna mast, koji se često sreće na ambalažama prehrambenih proizvoda. Hidrogenizovane biljne masti predstavljaju veštački zasićena ulja dobijena dodavanjem vodonika. Margarin i kikiriki puter su primeri proizvoda koji se hidrogenizuju kako bi se zadržali u čvrstoj formi. Ishrana koja se bazira na prekomernim unosom masti je jedan od glavnih faktora rizika za oboljenje od srčanih i vaskularnih bolesti. Taloženje masti na unutrašnjoj površini krvnih sudova dovodi do arteroskleroze oboljenja koje se manifestuje smanjenjem prohodnosti i elastičnosti krvnih sudova. |
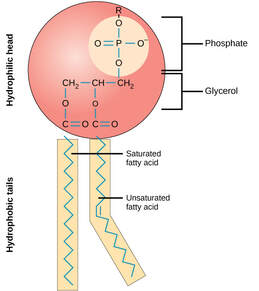
Fosfolipidi su po strukturi estri alkohola glicerola. Za 2 atoma ugljenika molekula glicerola vezane su 2 masne kiseline, dok je za treći atom vezana fosfatna grupa. To su amfipatični molekuli jer su na jednom kraju hidrofilni (fosfatna grupa je rastvorljiva u vodi), a na drugom hidrofobni (masne kiseline). Amfipatičnost omogućava njihovu karakterističnu orjentaciju u vodenom rastvoru.U živim ćelijama čine 25% svih lipida. Glavna uloga im je u obrazovanju ćelijskih membrani (fosfolipidni dvosloj).Fosfatidil-etanolamini ulaze u sastav bioloških membrana.Nalaze se i u nervnom i moždanom tkivu.U sastav kefalina (triv. naziv za ove fosfolipide) ulaze različite zasićene (14-18 C atoma) i nezasićene (18-22 C atoma) masne kiseline. Može se izolovati ekstrakcijom iz npr. semena soje.
| Lipidi prezentacija tmf | |
| File Size: | 143 kb |
| File Type: | |
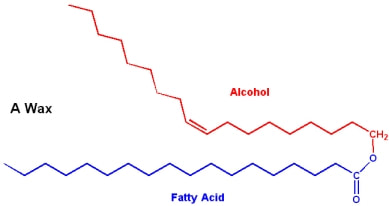
Voskovi su tip strukturnih lipida. Voskovi se sastoje od dugog lanca masne kiseline koja je povezana sa dugim lancem alkohola. Voskovi su vodnonepropusni i kod biljaka grade zaštitni omotač na spoljašnjoj površini. Osim kod biljaka voskovi obrazuju i zaštitne omotače i kod životinja. Cerumen koji se stvara u ušima i koji ima odbrambenu ulogu od mikroorganizma je vosak.
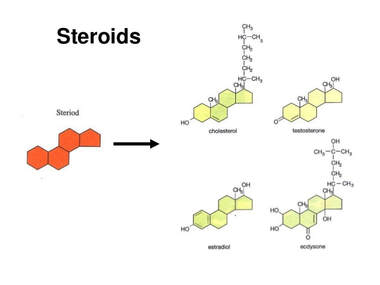
Steroidi se po građi razlikuju od svih navedenih lipida. Za razliku od prethodnih lipida u čiji sastav ulaze masne kiseline, steroide čine četiri povezana ugljenična prstena sa različitim hemijskim gurpama koje su vezane za njih .
Najpoznatiji steroid je holesterol. Holesterol se stvara u jetri i ulazi u sastav ćelijskih membrana. Od njega se sintetišu polni hormoni estrogen i testosteron, kao i vitamini D i K. Holesterol je neophodan u organizmu za mnoge metaboličke procese, ali u većoj količini može biti štetan.
Najpoznatiji steroid je holesterol. Holesterol se stvara u jetri i ulazi u sastav ćelijskih membrana. Od njega se sintetišu polni hormoni estrogen i testosteron, kao i vitamini D i K. Holesterol je neophodan u organizmu za mnoge metaboličke procese, ali u većoj količini može biti štetan.
Trepeni čine osnovu bioloških pigmenta , kao što je pigment vida retinal kod životinja i hlorofil kod biljaka. Takođe lipidi kao što su prostaglanidni spadaju u grupu važnih hemijskih glasnika u ćelijama.
Proteini ili belančevine su organski makromolekuli sačinjeni uglavnom od ugljenika, vodonika,kiseonika i azota. Ovi makromolekuli su građeni od monomera-amino kiselina koji su povezani petpidnim vezama. U sastav proteina ulaze 20 različitih aminokiselina. Sekvenca amino kiselina u proteinu definisana je u genima i sadržana u genetičkom kodu, koji određuje 20 amino kiselina.
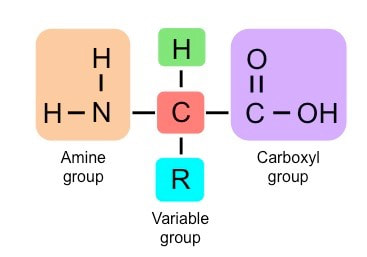
Aminokiseline su jedinjenja koja sadrže amino grupu (-NH2) i karboksilnu grupu (-COOH). Glavna razlika između amino kiselina je u bočnoj grupi R grupi koja je promenljiva (varijabilna). Promenljiva bočna grupa može biti jednostavna kao što je metil ili etil grupa ili složena(dugi ugljovodonični niz, aromatična jedinjenja). Razlike između R grupa aminokiselina određuju različite funkcije proteina.
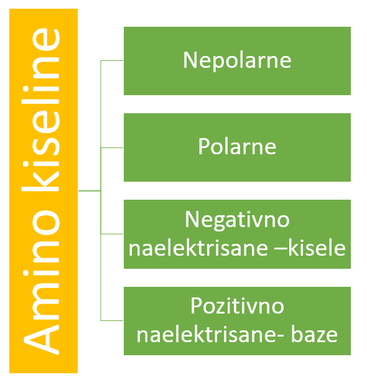
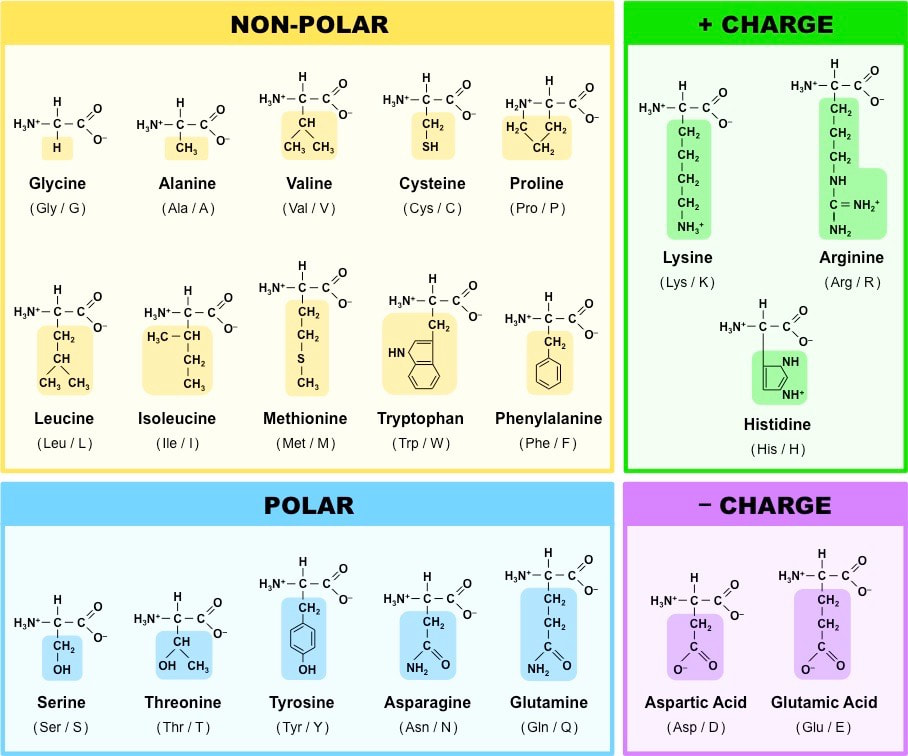
Na osnovu prirode bočne grupe amino kiseline se mogu svrstati u tri grupe:
1.Nepolarne amino kiseline- kao bočnu grupu sadrže nepolarnu hidrofobnu grupu.
2. Polarne amino-kiseline-kao bočnu grupu sadrže polarnu hidrofilnu grupu.
3. Naelektrisane amino-kiseline-kao bočnu grupu mogu da sadrže neku negativno naelektrisanu grupu (kisele) ili pak pozitivno naelektrisanu grupu (baze).
Biljke su jedini organizmi sposobni da stvaraju sve neophodne aminokiseline. Životinje i čovek mogu da sintetišu samo neke aminokiseline, dok ostale moraju da unose hranom. Te aminokiseline koje se moraju uneti hranom da bi organizam normalno funkcionisao nazivaju se esencijalne (bitne).
1.Nepolarne amino kiseline- kao bočnu grupu sadrže nepolarnu hidrofobnu grupu.
2. Polarne amino-kiseline-kao bočnu grupu sadrže polarnu hidrofilnu grupu.
3. Naelektrisane amino-kiseline-kao bočnu grupu mogu da sadrže neku negativno naelektrisanu grupu (kisele) ili pak pozitivno naelektrisanu grupu (baze).
Biljke su jedini organizmi sposobni da stvaraju sve neophodne aminokiseline. Životinje i čovek mogu da sintetišu samo neke aminokiseline, dok ostale moraju da unose hranom. Te aminokiseline koje se moraju uneti hranom da bi organizam normalno funkcionisao nazivaju se esencijalne (bitne).
Za čoveka esencijalne amino-kiseline su: valin, leucin, izoleucin, metionin, fenilalanin,treonin,tirozin, lizin, triptofan, arginin i histidin. Aminokiseline arginin, cistein, glicin, glutamin, histidin, prolin, serin i tirozin su uslovno esencijalne. One normalno nisu neohodne u hrani, ali moraju da budu dostupne delu populacije kao što su bebe, koje ne sintetišu dovoljne količine ovih kiselina.
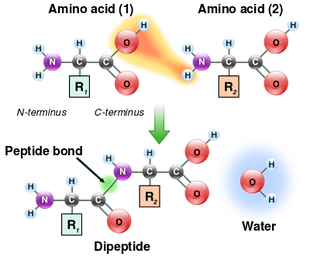
Kada su u vodenom rastvoru funkcionalne gurpe amino-kiselina su jonizovane tj. amino grupa nosi pozitivno naelektrisanje, dok je karboksilna grupa negativno naelektirsana. Pod određenim uslovima amino grupa jedne kiseline se vezuje za karboksilnu grupu druge amino kiseline i na taj način se formira petpidna veza uz izdvajanje vode.
Formiranje petpidnih veza kojima se pojedinačne amino-kiseline povezuju osnov je za nastajanje polipetpida. Petpidne veze su po tipu jake kovalentne veze. Spajanjem dve amino kiseline nastaje dipetpid, dok spajanjem većeg broja amino kiselina nastaje polipetpidni lanac. Svi proteini su građeni od jednog ili više polipetpidnih lanaca. Kao što smo već napomenuli redosled amino kiselina u polipetpidnom lancu nije slučajan već je definisan genima koji nose upustvo za određen protein.
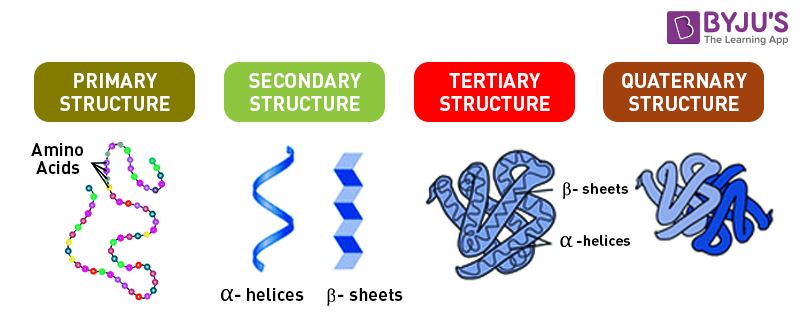
Postoje četiri nivoa strukture proteina . Primarna struktura određena je sekvencom (brojem i redosledom) amino kiselina u polipetpidnom lancu.Varijacije u sekvenci amino-kiselina u polipetpidnom lancu su izvor raznovrsnosti u građi i funkciji proteina. Svi ostali nivoi organizacije proteina su određeni primarnom strukturom određenog proteina. Svi nivoi strukture proteina iznad primarne predstavljaju zuzimanje specifičnog oblika u prostoru.
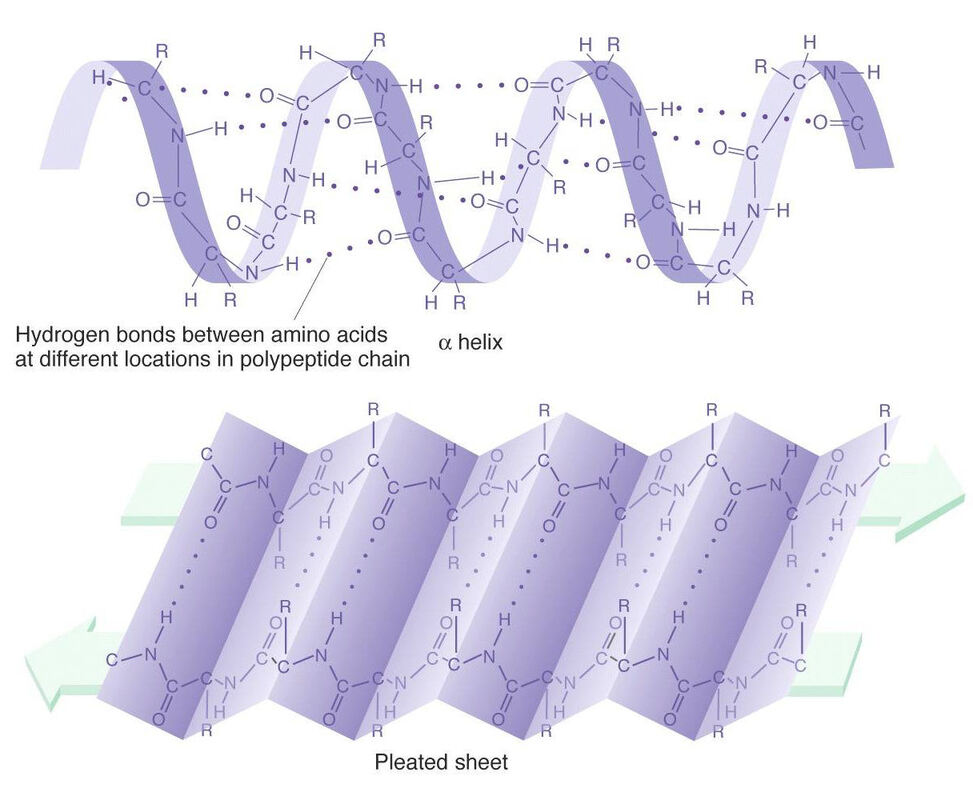
Sekundarna struktura određena je formiranjem vodoničnih veza između N-H grupe iz jedne petpidne veze i C=O grupe iz druge petpidne veze nesusednih amino kiselina.
Sekundarna struktura proteina ima dva osnovna oblika:
- Alfa zavojnica
- Beta ploča
Alfa zavojnica nastaje formiranjem voodnoničnih veza između atoma koji pripadaju svakoj četvrtoj amino kiselini. Kada se taj proces ponovi više puta na određenom delu proteina nastaje struktura zavojnice. Beta ploča se formira usled uspostavljanja vodoničnih veza između udaljenih delova polipetpidnog lanca, obrazujući strukturu ploče.
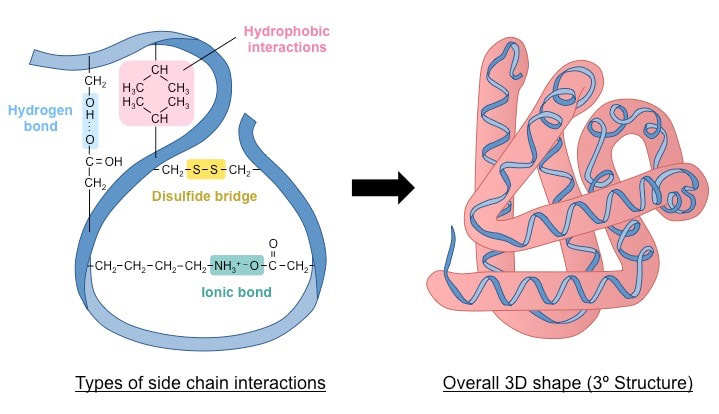
Tercijarna struktura proteina nastaje kada se polipetpidni lanac na određenim mestima , koja već nisu oformljena sekundarnom strukturom savija zauzimajući na taj način trodimenzionalni oblik. Oblik tercijarne strukture proteina određuju veze između R ostatka amino-kiselina. To mogu biti dislufidni mostovi (primer je kovalentna veza između SH- ostatka amino-kiselina cisteina), jonske veze (obrazuju se između pozitivno i negativno naelektirasnih bočnih ostataka amino-kiselina), kao i vodonične veze.
Kao rezultat prostornog organizovanja, polipetpid zadobija i specifičnu biološku aktivnost i za njega možemo koristiti termin protein- sve niže strukture predstavljaju polipetpidni lanac. Proteini mogu imamti fibrilarni ili globularni oblik. Fibrilarni proteini obično imaju strukturnu ulogu (npr. alfa keratin i kolagen koji grade kožu,krzno i vunu i kosu sisara, kao i beta keratin koji gradi perje,kožu,kandže i kljunove ptica i gmizavaca). Najveći broj proteina imaju globularni oblik.
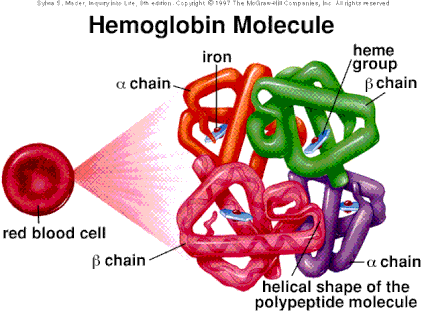
Kvaternernu strukturu nemaju svi proteini, ali je veliki broj proteina ima. Prisutna je kod proteina koji se sastoje od dva ili više polipeptidnih lanaca. Svaki od lanaca ima svoju tercijernu strukturu i označavaju se kao subjedinice. Subjedinice međusobno interaguju i povezuju se što kao rezultat proteinu daje kvaternarnu strukturu. Primer tako složenog proteina jeste hemoglobin. Hemoglobin je oligomer građen od 2 subjedinice, od kojih svaka sadrži po četiri polipetpidna lanaca.
Da li si znao: Ako bi se proteini lagano zagrevali, nastala toplota bi dovela do razgradnje slabih veza. Raskidanje veza dovodi do narušavanja sekundarne i tercijarne strukture tj. denaturacije proteina. Denaturacija proteina, za razliku od denaturacije molekula DNK je nepovratan proces (ponovnim hlađenjem protein neće povratiti svojstva) i denaturisan protein više nije biološki aktivan. Najbolji primer denaturisanog proteina je kuvano ili prženo jaje. |
Proteini imaju mnoge važne funkcije u svakom organizmu. Za proteine možemo reći da su izvršioci genetičke informacije. U zavisnosti od funkcije proteine delimo na:
- Transportne proteine (hemoglobin, hemocijanin)
- Odbranbene proteine (antitela)
- Hormone (insulin)
- Strukturne proteine (kolagen,elastin,keratin)
- Enzime
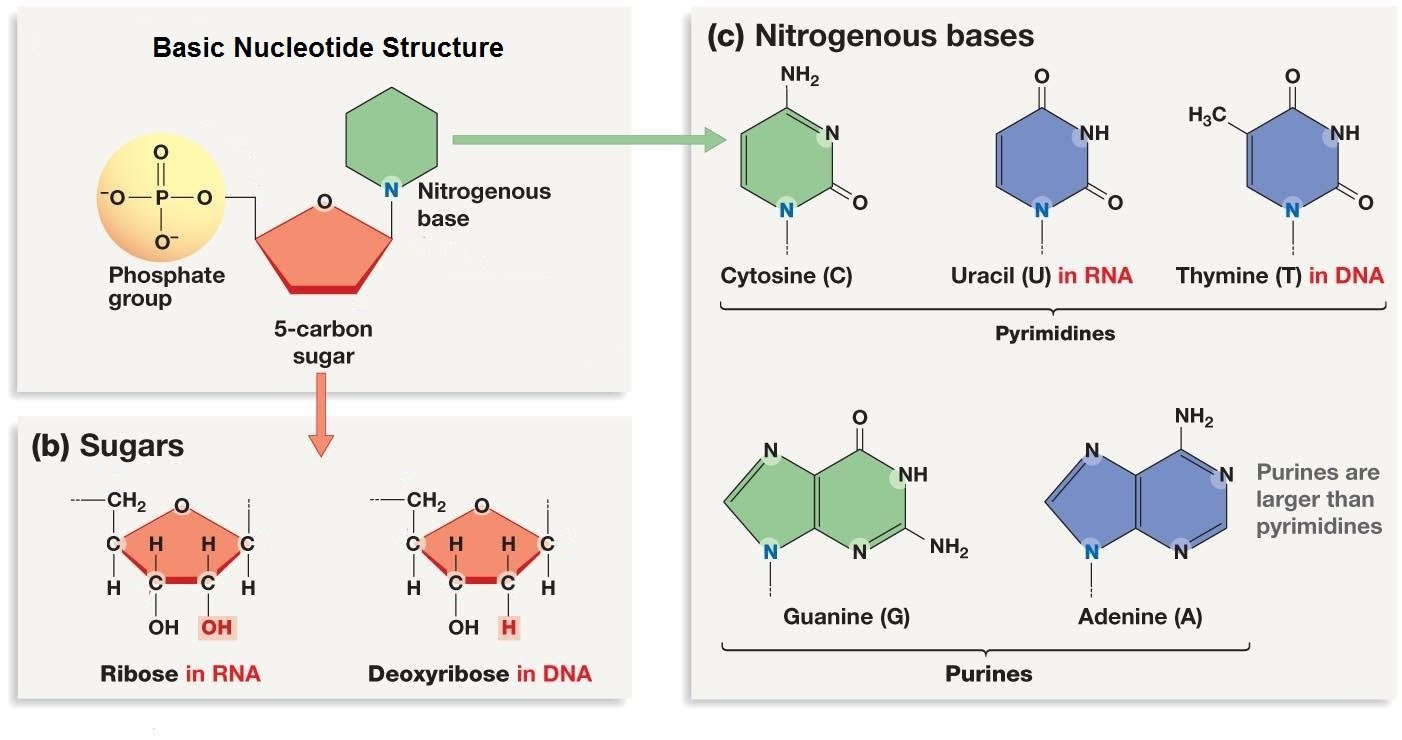
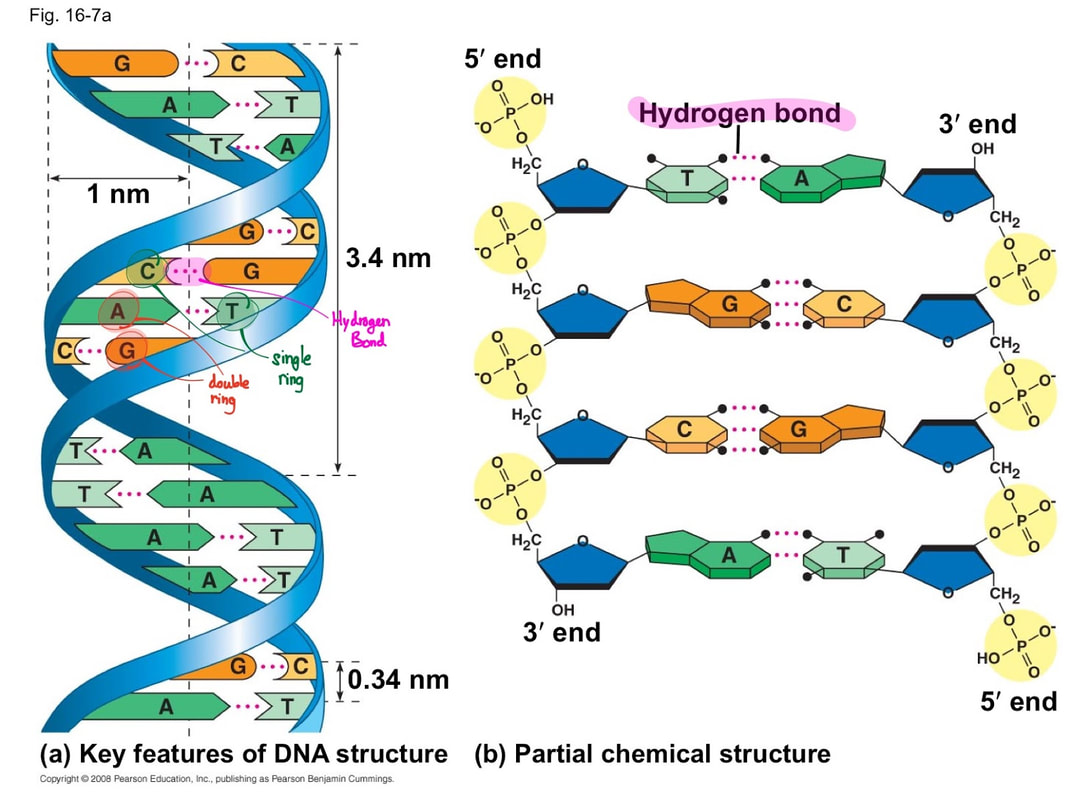
Nukleinske kiseline su polimeri nukleotida tj. lančani polinukleotidi. U nukleinske kiseline ubrajamo DNK (dezoksiribonukleinska kiselina) i RNK (ribonukleinsku kiselinu). Osnovna uloga nukleinskih kiselina je čuvanje i prenošenje genetičke informacije (kroz potomstvo) i prevođenje genetičke informacije u primarnu strukturu proteina.
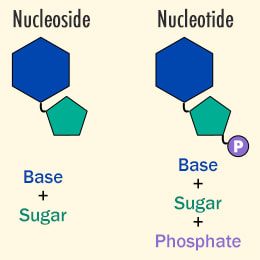
Nukleotidi su organski molekuli građeni od pentoznog šećera (riboze ili dezoksiriboze) povezanog sa azotnom bazom i sa fosfatnom grupom. Azotne baze mogu biti purinske ili piramidinske. Purinske baze su Guanin i Adenin, a piramidinske citozin,timin i uracil (koji je prisutan samo u RNK molekulu). U dvolančanom DNK molekulu uvek se komplementarno sparuju purinska baza jednog i priamidinska baza drugog lanca. Odnosno guanin se vodoničnom vezom vezuje za citozin, dok se adenin povezuje sa timinom.
Nespecifičnu okosnicu lanca (ista je kod svih nukleinskih kiselina), čine kovalentno povezana fosfatna grupa jednog i pentoza narednog nukleotida u nizu. Na jednom kraju lanca uvek se nalazi slobodna fosfatna grupa vezana za 5` ugljenikov atom pentoze. Taj kraj se označava kao 5`kraj polinukleotidnog lanca. Na drugom kraju se nalazi slobodna -OH grupa vezana za 3` ugljenikov atom pentoze i taj kraj se naziva 3`-kraj lanca. Specifičan tj. varijabilni deo nukleinskih kiselina čini vrsta azotne baze vezane za pentozu.
Primarna struktura nukleinskih kiselina odredjena je redosledom nukleotida. Sekundarna struktura je otkrivena od strane Vostona i Krika.Osnovu te strukture čini dvolančana zavojnica(spirala).Dva polinukleotidna lanca, koja čine ovu zavojnicu, su antiparalelna što znači da se naspram 5’ kraja jednog lanca nalazi 3’ kraj drugog, i obrnuto.
Da bi razumeli sekundarnu strukturu neophodno je razumevanje principa komplementarnog sparivanja.
U dvolančanom molekulu DNK uvek se vodoničnim vezama povezuju purinska baza jednog sa piramidinskom bazom drugog molekula. Kako su RNK molekuli građeni uglavnom od jednog lanca , oni mogu samo pod nekim slučajevima zauzeti sekundarnu strukturu. RNK može zauzeti sekundarnu strukturu u prostoru, kada se formiraju vodonične veze po principu komplementarnosti baza, ali samo u ograničenom delu jednog lanca.
Na osnovu molekulske mase DNK i podatka da jedan puni zavoj ima dužinu od 3,4 nm, lako se može izračunati ukupna dužina ispružene dvolančane zavojnice DNK u nekoj ćeliji. Tako, ukupna dužina dvolančene DNK u jednoj jedinoj ćeliji čoveka iznosi oko 2 m. Dužina potpuno ispružene DNK najvećeg ljudskog hromozoma (hromozom 1) iznosi 85 mm.Treba imati u vidu da je prečnik tipične ćelije oko 20 mikrometara, a njenog jedra 5-10 mikrometara. Tercijerna struktura predstavlja pakovanje DNK pomoću histonskih proteina. Prilikom pakovanja negativno naelektirsana DNK se obmotava oko pozitivno naelektirsanih histonskih proteina. Hromozomi su tvorevine karakterističnog oblika koje se pojavljuju u jedru eukariota samo tokom ćelijske deobe. U periodu između ćelijskih deoba DNK se nalazi u obliku hromatina.
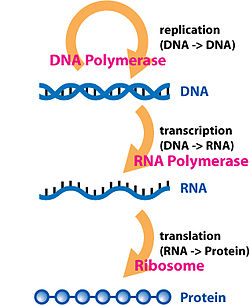
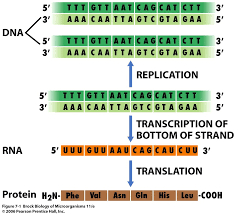
DNK molekul je isključivo informacioni molekul. Informacija koju nosi DNK molekul je određena brojem i redosledom nukleotida. U procesu replikacije uz pomoć enizima DNK može da se umnoži na način da se stvori istovetna kopija DNK. U procesu replikacije se informacija sa DNK prenosi na DNK, međutim za sintezu proteina je neophodno da se informacija prenese sa DNK na RNK. Procesom transkripcije (prepisivanja) informacija sa DNK molekula može da se prenese na sva 3 tipa RNK molekula. Deo molekula koji se sa DNK prepisuje na RNK naziva se gen. Transkripcija DNK je prvi korak u ekspresiji gena, pri čemu se informacija iz gena koristi za sintezu funkcionalog proizvoda kakav je protein. Sinteza iRNK počinje kada je ćeliji potreban određeni protein. Cilj ovoj procesa jeste da se napravi kopija sekvence DNK, odnosno, kopija gena. Glavni enzim u ovom procesu je RNK-polimeraza. Ona kao šablon koristi jedan lanac DNK za sintezu komplementarnog lanca RNK (naspram adenina u DNK postavlja se uracil u RNK, a naspram guanina – citozin i obrnuto). Triplet nukleotida na iRNK naziva se kodon. Kodon određuje tačno jednu amino-kiselinu u polipetpidnom lancu. Proces translacije (sinteze proteina )se odvija u ribozomima. U ribozomima se informacija sa iRNK čita kodon po kodon. tRNK je prevodilac informaicje sa jezika nukleotida na jezik aminokiselina. Naime tRNK u svojoj primarnoj strukturi nosi antikodon(triplet nukleotida koji je komplementaran kodonu sa iRNK molekula). Antikodon određuje tačno jednu amino-kiselinu koju će tRNK doneti sa sobom do ribozoma i po principu komplementarnosti anitkodon će se vezati za kodon, a doneta amino kiselina će se dodati rastućem polipetpidnom lancu.